Sicurezza dei farmaci testati
Perché i farmaci hanno ancora effetti collaterali nonostante i test di sicurezza?
Tutti gli studi portano solo a una relativa sicurezza, e si cerca di valutare i rischi nel miglior modo possibile al fine di sviluppare un farmaco il più sicuro possibile. La sicurezza al cento per cento non può essere garantita.
Gli effetti negativi possono anche essere influenzati dallo stile di vita. Per esempio, i pazienti che consumano molto alcol possono manifestare effetti collaterali diversi rispetto alle persone che bevono meno alcol o non ne bevono affatto. Devono essere prese in considerazione anche le possibili interazioni con altri farmaci o con altre malattie del paziente.
Anche la diversità genetica dei pazienti gioca un ruolo. Le differenze genetiche significano che il metabolismo differisce da persona a persona e che un principio attivo viene metabolizzato in modo diverso. Questo può essere la causa di rari effetti collaterali. Pertanto, può succedere in singoli casi che effetti collaterali non riscontrati negli studi clinici si manifestino anche con farmaci già registrati..
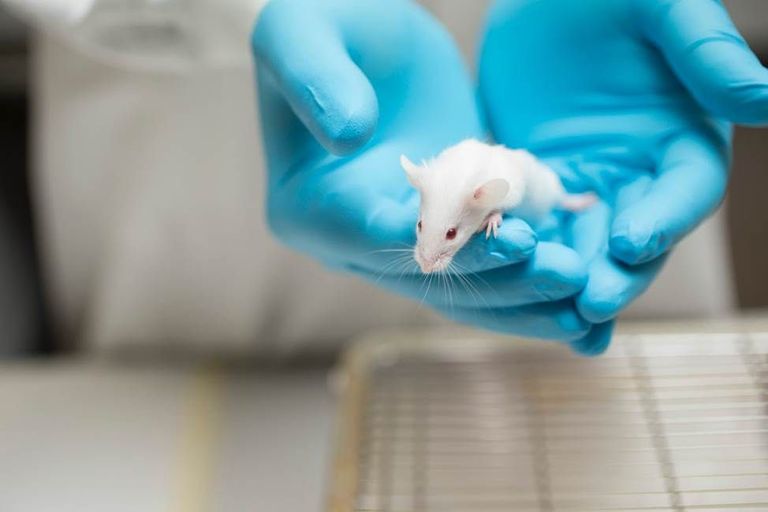
I test di sicurezza negli studi sugli animali sono solo la prima fase di molti test di sicurezza prima che un farmaco venga registrato. Questo è seguito da ulteriori test sugli esseri umani in studi clinici. Da un lato, gli esperimenti sugli animali vengono utilizzati per testare il il principio attivo e per scoprire se un farmaco funziona davvero e, se sì, come. D'altra parte, viene verificato se un principio attivo è sufficientemente sicuro per essere usato nell’uomo. Solo dopo questa fase di test il principio attivo viene accuratamente testato sull'uomo, e se si dimostra efficace e sicuro nei successivi studi clinici su persone sane o pazienti, il principio attivo può essere registrato come farmaco. Questo processo richiede di solito molti anni.
Il caso del talidomide non dimostra che i test sugli animali danno un falso senso di sicurezza?
Per quanto buoni possano essere i test, si può solo ridurre il rischio di effetti collaterali indesiderati. Ma non si può mai escluderli completamente. Tra la fine degli anni '50 e l'inizio degli anni '60, molti bambini sono nati con gambe o braccia mutilate dopo che le loro madri avevano assunto il sonnifero talidomide durante la gravidanza. La talidomide, il principio attivo del sedativo e sonnifero talidomide, è stata testata sui roditori prima di essere introdotta sul mercato negli anni '50.
Il danno che la talidomide ha causato agli embrioni umani nelle prime settimane di gravidanza non è stato osservato nei test sugli animali. A quel tempo, i test su animali gravidi non erano ancora una pratica standard. Poco dopo lo scandalo della talidomide, furono condotti esperimenti su conigli gravidi che che provocarono esattamente le deformità che si erano verificate negli esseri umani.
Se la talidomide fosse già stata testata su animali gravidi, molto probabilmente si sarebbero notati i cambiamenti negli embrioni animali e si avrebbe quindi saputo che la sostanza provoca questi effetti negativi sugli embrioni. Tali test (teratologici) sono oggi una parte obbligatoria dello sviluppo preclinico di un farmaco.
Nei test cellulari, la talidomide non è né tossica né modifica il genoma. Con i metodi alternativi oggi disponibili, probabilmente le malformazioni provocate dalla talidomide non sarebbero state scoperte.. Questo spiega anche perché non è possibile testare un principio attivo completamente senza l'uso di animali.

